di Marco de’ Francesco♦ La digital transformation del pharma, biopharma e medicale è favorita anche dalla necessità delle compliance con le strette regole esistenti a salvaguardia dell’ industria della salute. La consulenza manageriale e digitale dell’ azienda guidata da Teresa Minero. Se ne parla a Milano in un convegno organizzato da Messe Frankfurt in vista di Sps Parma e moderato dal direttore di industria italiana Filippo Astone
Tre direttrici di sviluppo di LifeBee, azienda milanese che si occupa della trasformazione digitale delle industrie del Life Science, e cioè pharma, biopharma e medicale. Anzitutto, la focalizzazione sugli analytics; poi, l’espansione in mercati “contigui”, come il cosmetico e quello degli integratori; e infine l’internazionalizzazione. Ora, il Life Science è un settore fortemente regolamentato da autorità nazionali, europee e mondiali. Ciò significa che la digitalizzazione delle aziende-clienti va attuata tenendo conto di precise misure relative alla riservatezza e alla salute dei consumatori. E, dal 9 febbraio, con l’entrata in vigore di una direttiva europea, di regole anticontraffazione: per i prodotti venduti all’estero, è prevista la tracciabilità digitale del farmaco, azione che impatterà sui processi produttivi nonché sull’intera filiera, dallo shopfloor sino al farmacista.
L’impressione è che sul punto le industrie farmaceutiche nostrane non siano ancora del tutto pronte; tuttavia, la norma è destinata a produrre una spinta ulteriore verso la digital transformation, seppure in maniera un po’ forzosa. Ma LifeBee ha una sua strategia, sperimentata in 15 anni, quella di procedere su tre fronti al contempo, integrando gli uni e gli altri: innovazione, compliance e processi operativi. Peraltro il 26 febbraio si terrà, a Milano, il convegno “Pharma 4.0: processi eccellenti e tecnologie abilitanti per il futuro del farmaceutico italiano“, dove sarà offerta una panoramica di nuove applicazioni in tema di digital trasformation. L’evento, moderato nella mattinata dal direttore di Industria Italiana Filippo Astone, è organizzato da Sps Ipc Drives, fiera dell’automazione legata all’espositore globalizzato Messe Frankfurt, ed è realizzato grazie alla Affiliata Italiana di Ispe, la più grande associazione globale no profit dedicata ai professionisti del farmaceutico e delle scienze della vita, di cui Teresa Minero, founder e Ceo di LifeBee è Chair Italy nonché membro dell’Eu leadership team di Ispe.

La strategia olistica nella digitalizzazione del Life Science
Va anzitutto ricordato che il principale settore di riferimento del Life Science, il farmaceutico, ha fatto registrare in questi ultimi anni nel Belpaese una crescita considerevole. L’anno scorso, con 31,2 miliardi di fatturato, ha scalzato la Germania (30 miliardi) conquistando il gradino più alto sul podio continentale. È composto perlopiù da imprese medie e medio-grandi. Gli investimenti per addetto sono del 390% più alti della media del manifatturiero, e superano anche la media dei settori medium e high tech.
LifeBee è una piccola azienda, con 5 milioni di fatturato realizzato per l’80% in madrepatria, ed è costituita da una trentina di esperti per lo più dipendenti. Gli inizi, 15 anni fa, come start-up. «Ho riunito dei giovani colleghi dalla mente aperta – afferma la Minero – che ancora oggi lavorano in LifeBee». Tra allora ed oggi, più di 60 clienti per oltre 400 progetti. Ma perché le industrie farmaceutiche si rivolgono, per la consulenza digitale e manageriale, a LifeBee? «Le grandi società della consulenza internazionale non rappresentano per noi una vera e propria concorrenza perché si occupano normalmente di processi amministrativi e gestionali più “alti”, mentre LifeBee si dedica a tutti quei processi di “nicchia”, ma soggetti alle stringenti regolamentazioni di settore: dalla produzione, al controllo qualità, alla assicurazione qualità, alla logistica, al regolatorio, alla clinica e alla farmacovigilanza (cioè la gestione delle reazioni avverse del farmaco a partire dalla ricerca clinica fino alla commercializzazione). Sono tutte attività che richiedono conoscenze specifiche di processo e di compliance e esperienza».
E poi, secondo la Minero, c’è un altro motivo. «Ciò che differenzia LifeBee da altri player è che noi pensiamo da sempre che innovazione digitale, compliance e processi operativi debbano marciare insieme; spesso invece le aziende tendono a cercare soluzioni ai problemi in modo separato sui tre diversi fronti. Ciò che l’operato di LifeBee mette in evidenza è che agire in modo non coordinato può essere controproducente: se si interviene solo sulla compliance regolatoria si rischia di irrigidire i processi aziendali e d’altra parte l’adozione delle tecnologie abilitanti del 4.0 senza ripensare i processi può comportare la generazione di costi e inefficienze e impedire il conseguimento dei risultati attesi. I processi nel Life Science vanno migliorati, tenendo bene a mente la centralità del ruolo del digitale unita alla intelligente applicazione delle regole di compliance».
Non solo luci nella trasformazione digitale del farmaceutico
Secondo la Minero «dobbiamo essere consapevoli che quanto fatto fin qui non è ancora “Pharma 4.0”. Non è solo nuove macchine produttive e automazione, ma anche tecnologie abilitanti di facile utilizzo, flussi di informazione integrati e condivisi, processi rivisti e in continua evoluzione, apertura mentale al cambiamento continuo, anche turbolento. Anche per questo abbiamo oggi, in tutta l’industria, un problema scottante di competenze: se è importante fare formazione sui giovani per creare i nuovi profili professionali necessari al 4.0, lo è persino di più farla sui manager, che sono gli attuali decisori degli investimenti verso il Pharma 4.0».
Le tecnologie più richieste: gli analytics. I progetti pilota
Secondo la Minero, con il Piano Calenda le aziende del Life Science hanno compiuto considerevoli passi in avanti quanto a digitalizzazione, con importanti investimenti. Macchine e impianti integrati, sistemi informatizzati per gestire e controllare la funzione produttiva dell’azienda (Mes), apparati di analisi della qualità, e tanto altro. Ora la richiesta delle aziende-clienti, quanto a tecnologie specifiche, è relativa al mobile, al Cloud e soprattutto agli analytics. Questi sono strumenti software che consentono, raccogliendo e esaminando grandi volumi di dati, di trovare correlazioni tra informazioni, determinare trend e comportamenti stagionali, analizzare serie storiche, segmentare clienti, fornire indicazioni sulle condizioni di mercato e simulare scenari economici. Ma anche di definire decisioni sul portafoglio, di prevedere gli indicatori di budget, di determinare una maggiore efficienza nei processi produttivi e nelle sperimentazioni cliniche, con tempi di commercializzazione più rapidi. Uno degli obiettivi è di rendere l’attività decisionale più veloce rispetto alla concorrenza.
Questa tecnologia sta assumendo un tale rilievo che LifeBee la menziona come la prima tra le direttrici di sviluppo dell’azienda. «E poi ci sono progetti-pilota – afferma la Minero – ai quali stiamo collaborando». Uno è con una grande multinazionale del farmaceutico. « un caso di utilizzo di Augmented Reality applicato al training in area sterile». Il contesto è ovviamente simulato, ma chi indossa il particolare visore impara a muoversi e ad operare come se stesse agendo sul campo. Impara dai propri errori, con una formazione «altrimenti non possibile perché a rischio contaminazione». Per le industrie di settore il risparmio è davvero considerevole, perché realizzare e mettere a disposizione aree “asettiche” ha dei costi molto alti.
La serializzazione accelera la trasformazione digitale
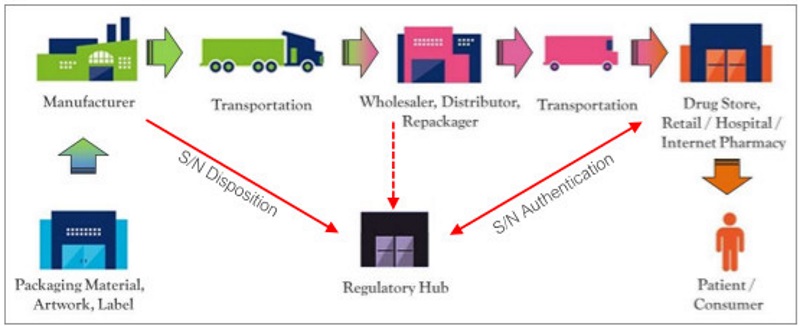
Sul processo di trasformazione digitale delle industrie farmaceutiche sta impattando un altro fenomeno, la cosiddetta “serializzazione”. Consiste nell’assegnazione di numeri univoci che rendono tracciabili i singoli articoli o unità in modo da verificare a monte e a valle che tutti i prodotti integrino caratteristiche di sicurezza. Serve cioè ad evitare furti, sprechi e soprattutto danni alla salute derivanti da medicinali contraffatti. È stata imposta a livello continentale con la direttiva 2011/62/UE (nota come “Falsified Medicines Directive”, Fmd) entrata in vigore il 9 febbraio 2019. L’Italia e la Grecia, dal momento che già disponevano di un sistema di verifica “con bollino”, godono di un grace period di sei anni ma solo per il loro mercato interno; e le aziende italiane esportano l’80% della loro produzione.
Perciò, quando le aziende italiane vendono nei Paesi dell’Unione, devono far sì che i farmaci siano dotati di un Data Matrix, un codice particolare contenente almeno quattro informazioni: numero di lotto, data di scadenza, numero di articolo di commercio globale (Gtin) e un numero di serie casuale. I produttori codificano i loro prodotti e trasmettono i dati a un hub centrale dell’Ue gestito dall’European Medicines Verification Organization (Emvo). Queste informazioni sono poi inoltrate a database nazionale; e i farmacisti controllano i codici collegandosi ad essi. Ogni articolo con dati univoci determina per gli attori della filiera e per il paziente finale un accesso a informazioni di cui tener conto nel corso del tempo.
«Per serializzazione in ambito farmaceutico possiamo parlare di integrazione verticale e orizzontale dei processi. Nel primo caso, perché le informazioni raccolte dalla sensoristica sono analizzate a livello di impianto, a livello corporate e quindi di enti regolatori; nel secondo perché rilevano sui processi della catena logistica, in tutti i passaggi dal confezionamento alle farmacie dove il prodotto viene venduto. È una trasformazione complessa, perché le modifiche riguardano tutti i dipartimenti dell’industria. In un certo senso si deve ammettere che la complessità della serializzazione ha abbattuto dei silos. All’interno delle aziende, dall’Information Technology alla produzione alla logistica alla compliance, sono tutti coinvolti».
Per ora LifeBee ha aiutato 20 aziende che si sono portate avanti con la serializzazione. Va peraltro sottolineato che l’Ue non è l’unica ad aver agito su questo fronte: «la Turchia l’ha fatto qualche anno fa, con un proprio modello di tracciabilità, e altrettanto stanno facendo USA e Russia, con tempistiche e modelli propri.» In ogni caso, il problema delle aziende non è stato quello di cambiare macchine di confezionamento non adeguate alla stampa del Data Matrix, quanto quello della modifica dei processi operativi nel loro insieme. Anche il passaggio delle informazioni all’It, in Cloud “regolati” a garanzia della salute dei pazienti e della confidenzialità dei dati, è peculiare. Apparentemente, le aziende farmaceutiche nostrane non sono del tutto pronte all’adozione della direttiva europea. E si tratta di processi che richiedono due anni.

L’espansione nel settore nutraceutico e cosmetico
Con il termine nutraceutico ci si riferisce a prodotti che contengono principi nutrienti con effetti benefici sulla salute: proprietà preventive, riequilibrative e protettive a livello psicofisico. Non solo gli integratori, ma anche i cosiddetti alimenti funzionali o farmalimenti, e cioè sostanze biologiche solitamente concentrate: acidi insaturi omega 3 o omega 6, l’acido folico, la carnitina a tante altre. Anche questo mercato, come quello della cosmesi, è regolamentato, in particolare da una norma del 2006 del Parlamento Europeo. «L’asticella della regolamentazione è un po’ più bassa di quella del farmaceutico, ma è comunque un riferimento di grande rilievo» – afferma la Minero. In pratica, questi mercati affini al farmaceutico sono quelli adatti per tentare la strada dell’espansione, perché l’esperienza accumulata nel life science può esservi trasferita.
L’internazionalizzazione
Attualmente LifeBee realizza il 20% del proprio fatturato all’estero, in particolare in Usa, Svizzera, Regno Unito, e Francia. «Ora – afferma la Minero – vogliamo espanderci all’estero, spinti dall’importanza che sta assumendo un po’ dovunque la trasformazione digitale e il 4.0 negli ambiti regolati del Life Science. Stiamo valutando possibili collaborazioni con importanti aziende internazionali. Sono poche aziende al mondo che hanno le nostre competenze».

[boxinizio]
Il Convegno Pharma 4.0: processi eccellenti e tecnologie abilitanti per il futuro del farmaceutico italiano
Si terrà nella sede del Gruppo 24 Ore, in via Monte Rosa 91, dalle 10 in Sala Bianchi. La mattinata offrirà una panoramica di applicazioni concrete di Industria 4.0 nel settore farmaceutico, coinvolgendo le aziende di riferimento e i fornitori di tecnologie digitali e di automazione. Il pomeriggio ospiterà gli studenti per una sessione dedicata alla formazione, parola chiave della prossima edizione di SpsItalia, al fine di condividere le competenze necessarie per lo sviluppo del settore in ottica digital transformation. Dopo i saluti di benvenuto della vice president marketing&events Messe Frankfurt Italia Francesca Selva e della Minero, i lavori saranno aperti dal docente del dipartimento di energia del Politecnico di Milano Cesare Maria Joppolo.
Il convegno (qui il link per l’iscrizione), nella mattinata, sarà moderato dal direttore di Industria Italiana Filippo Astone. Interverranno il consigliere e vice presidente Fondazione Smith Kline Giuseppe Recchia, il manager Menarini David Smaldone, il M&Q I.T. /Process Automation Director Sesto Fiorentino and Global Data Integration and Analytics Eli Lilly Italia Gian Mauro Brozzi, la manager di Lilly Italia Rachele Donati. Alla successiva tavola rotonda, verso le 12, saranno presenti Marco Banti di Abb, Manuela Bellavigna di Schneider Electric, Claudio Brusatori di Porsche Consulting, Maurizio Burani di Lenze, Andrea Corbelli di B&R, Alessandro Favero di Phoenix Contact, Alberto Griffini di Mitshbishi Electric Europe, Marco Chesi di Oracle e Vincenzo Tampellini di Beckhoff Automation. Nel pomeriggio, dalle 14, con la moderazione del docente del dipartimento di elettronica Giambattista Gruosso, si terrà un incontro formativo verso Sps Drives Italia, la fiera dell’automazione che si terrà a Parma tra il 28 e il 30 maggio. Tra le personalità che interverranno, il filosofo Franco Bolelli e il rappresentante Ispe Young Professional Federico Poli.
Ispe
l’International Society for Pharmaceutical Engineering è la più grande associazione no-profit al mondo a servizio dei suoi membri, che rappresentano tutte le aree scientifiche e tecniche dell’industria farmaceutica: ingegneri, microbiologi, chimici; rappresentanti di produzione e sviluppo di processi; farmacisti, personale di regolamentazione e formazione, università, fornitori e altri professionisti. L’associazione è stata fondata nel 1980. Il presidente in USA e nel 1992 in Italia è John Bournas. Il Chair attuale è James A. Breen, Jr. La sede principale è a North Bethesda, in Usa. Quanto all’attività dell’Ispe, si vuole garantire l’aggiornamento tecnico e normativo dei membri sul ciclo di vita dei farmaci, incrementare e condividere le conoscenze, e altro». Ci ha detto a proposito la Minero: «Ispe ha quasi 20mila associati nel mondo e poco meno di 500 in Italia.Una grande squadra: io sono presidente nazionale dal 2016, parte del Leadership Team europeo, e componente dello Steering Committee su Pharma 4.0 a livello globale».

















